TESTS GÉNÉTIQUES
Diagnostic Pré-Implantatoire (DPI)
Le diagnostic pré-implantatoire (DPI), également appelé PGT (Preimplantation Genetic Testing), est une technologie avancée de génétique reproductive qui permet d’analyser les embryons obtenus par FIV avant leur transfert dans l’utérus.
Objectifs des tests génétiques préimplantatoires
Cette approche permet :
- d’identifier les embryons chromosomiquement normaux
- de prévenir la transmission de maladies génétiques héréditaires
- de réduire le risque de fausses couches
- d’augmenter les taux d’implantation
- d’optimiser les chances de naissance d’un enfant en bonne santé.
Au Centre IRIFIV, le PGT est proposé selon des indications médicales précises et s’intègre dans une stratégie personnalisée et scientifiquement encadrée.
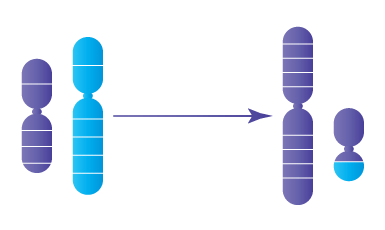
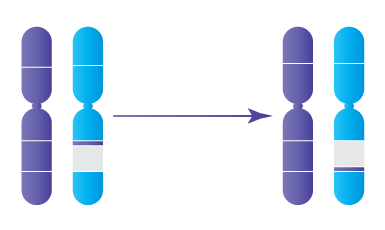
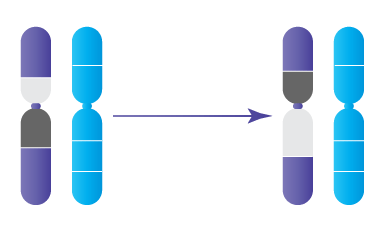
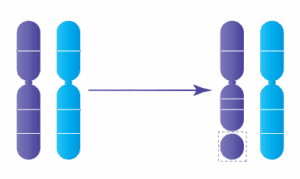
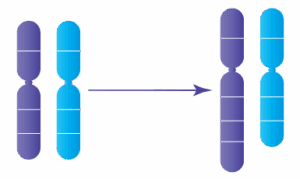
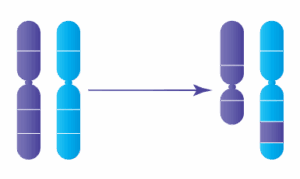
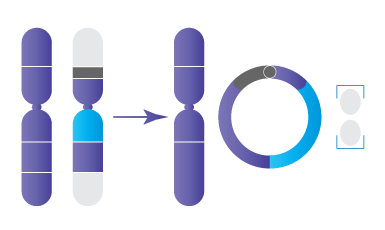
Comprendre les chromosomes et l’aneuploïdie
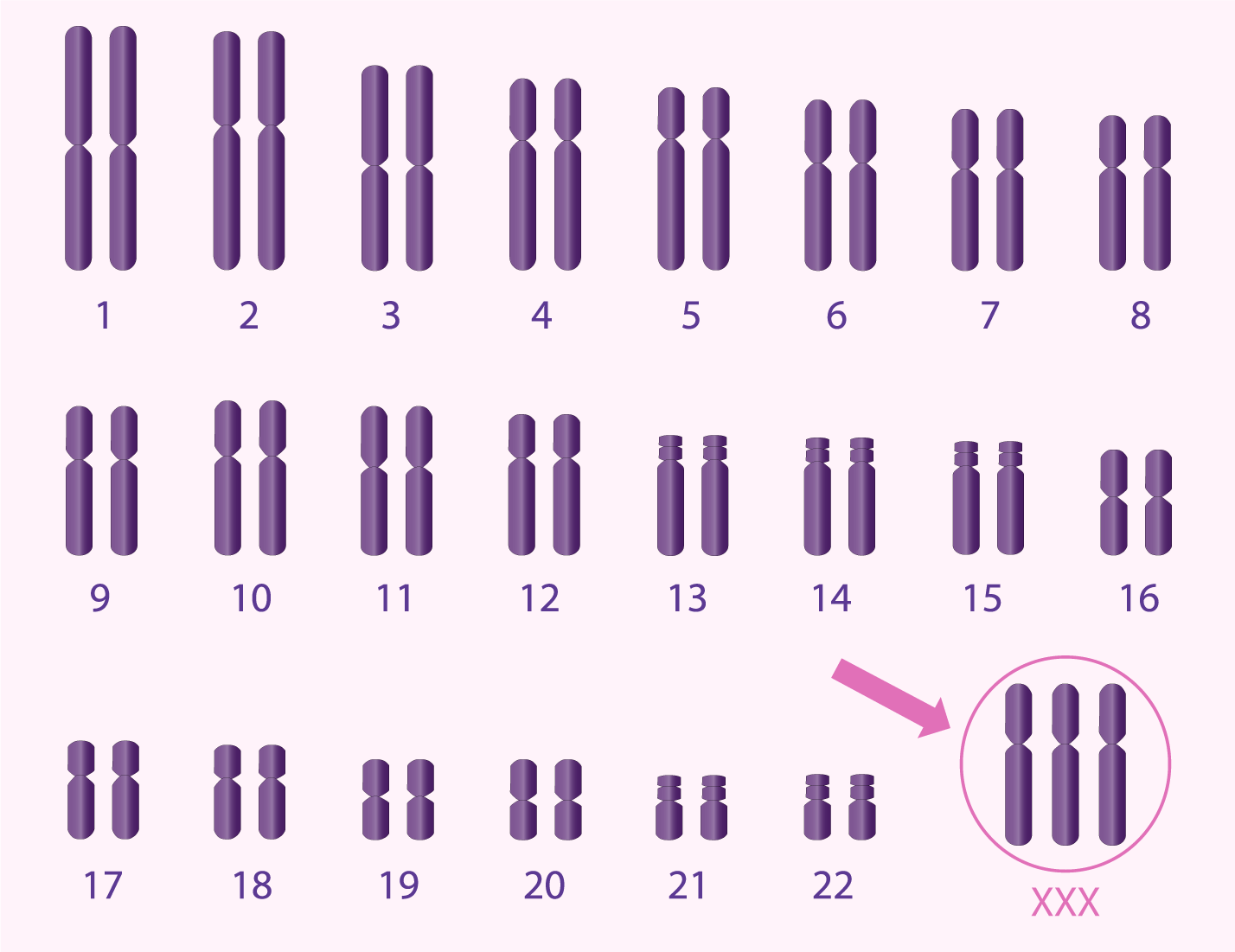
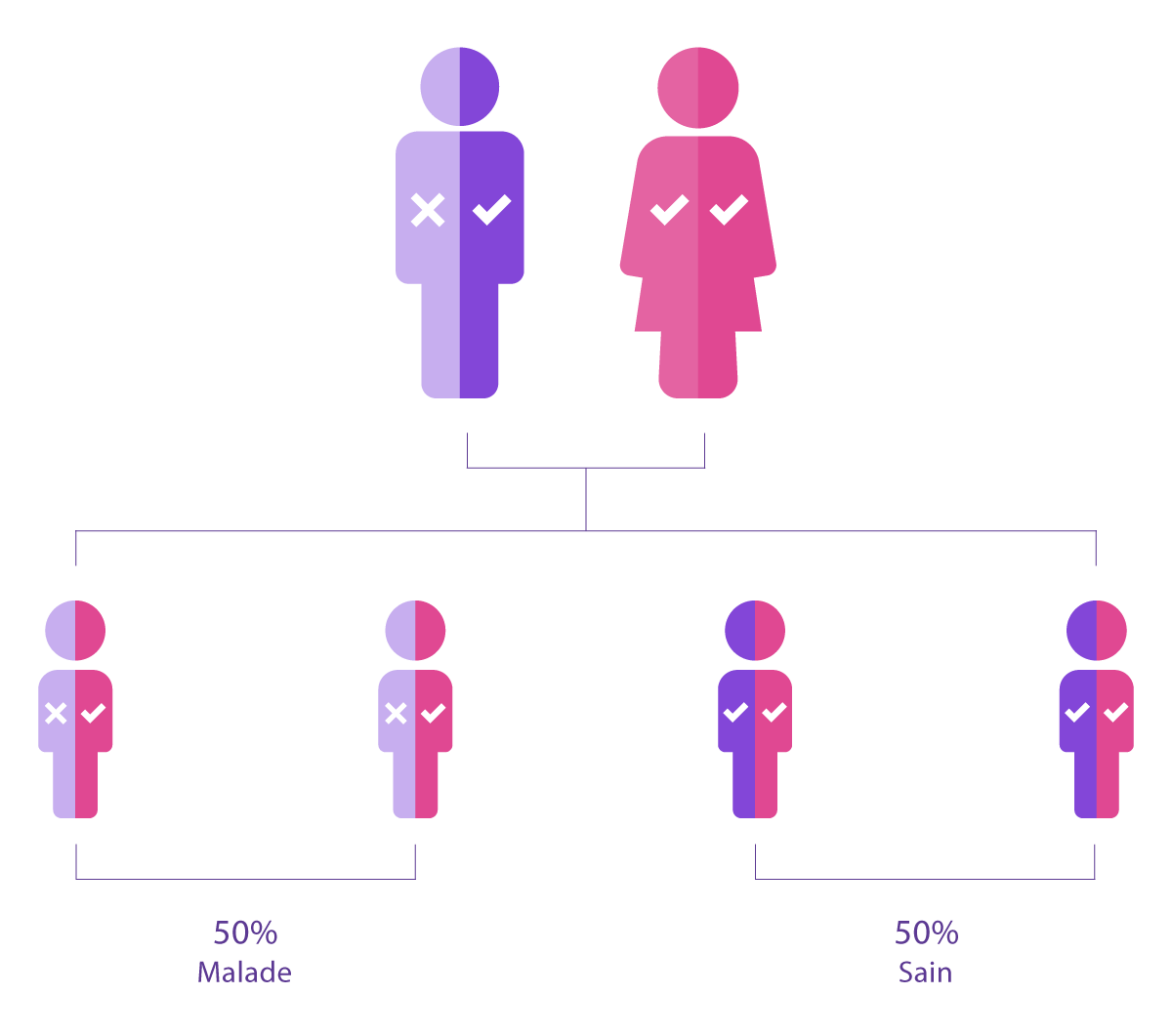
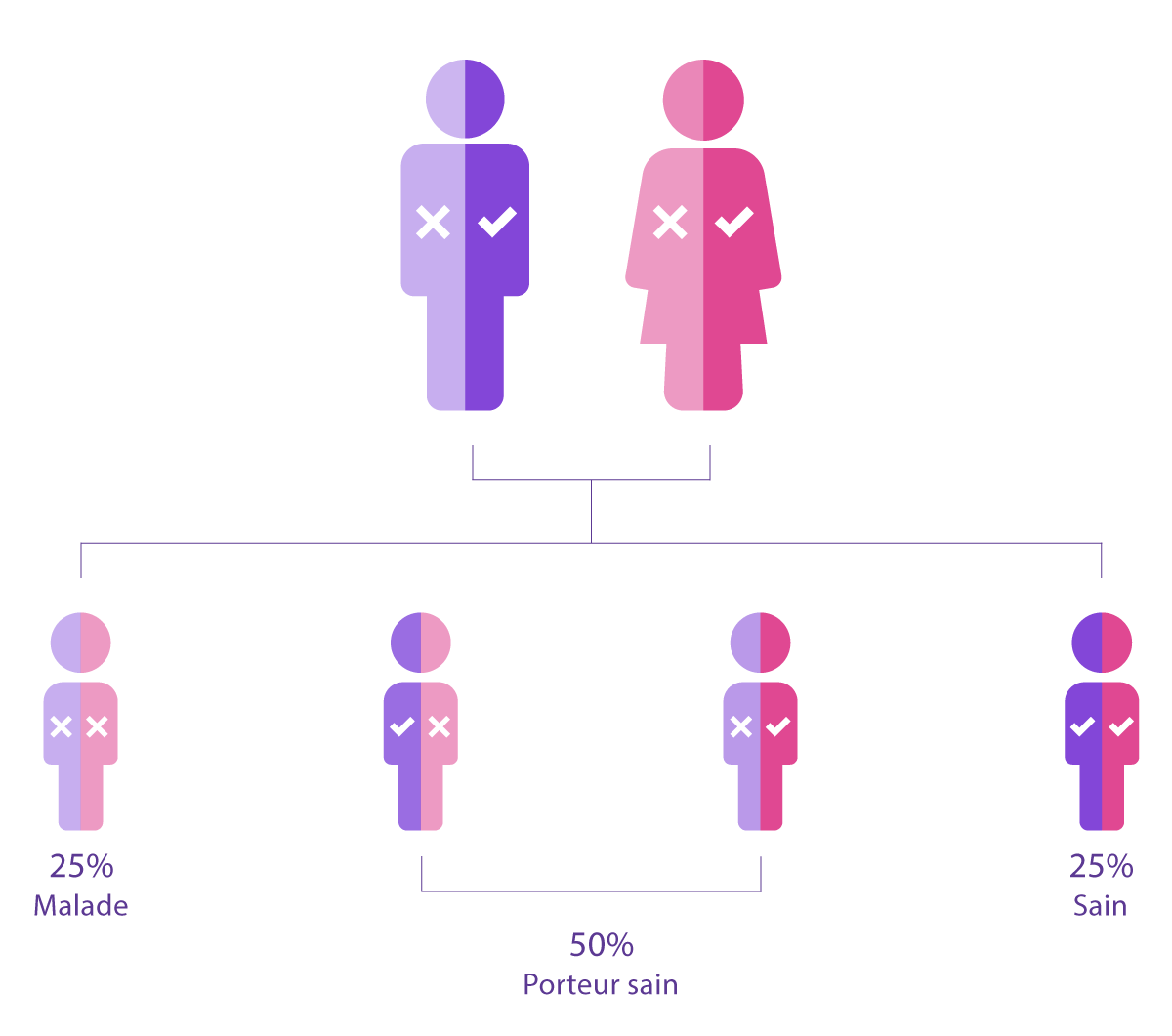
Chaque embryon humain normal contient 46 chromosomes, organisés en 23 paires : 23 proviennent de l’ovocyte et 23 du spermatozoïde. Une anomalie du nombre de chromosomes est appelée aneuploïdie.
Les embryons aneuploïdes :
- s’implantent difficilement
- sont responsables de nombreuses fausses couches précoces
- peuvent entraîner certaines anomalies congénitales
Le risque d’aneuploïdie augmente avec l’âge maternel. À partir de 38,40 ans, plus de la moitié des embryons peuvent présenter une anomalie chromosomique, expliquant l’augmentation du risque de fausse couche ou de pathologies comme :
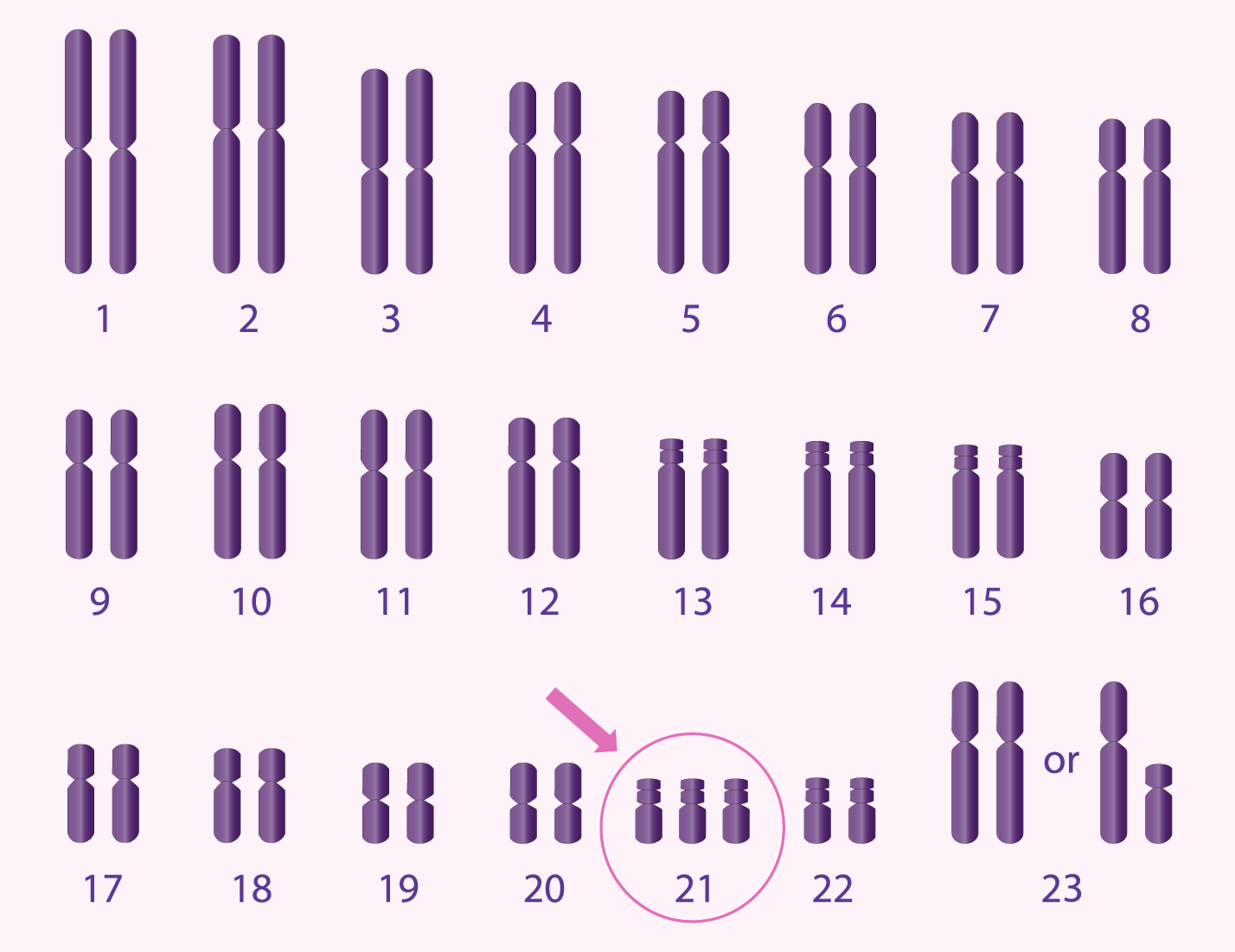
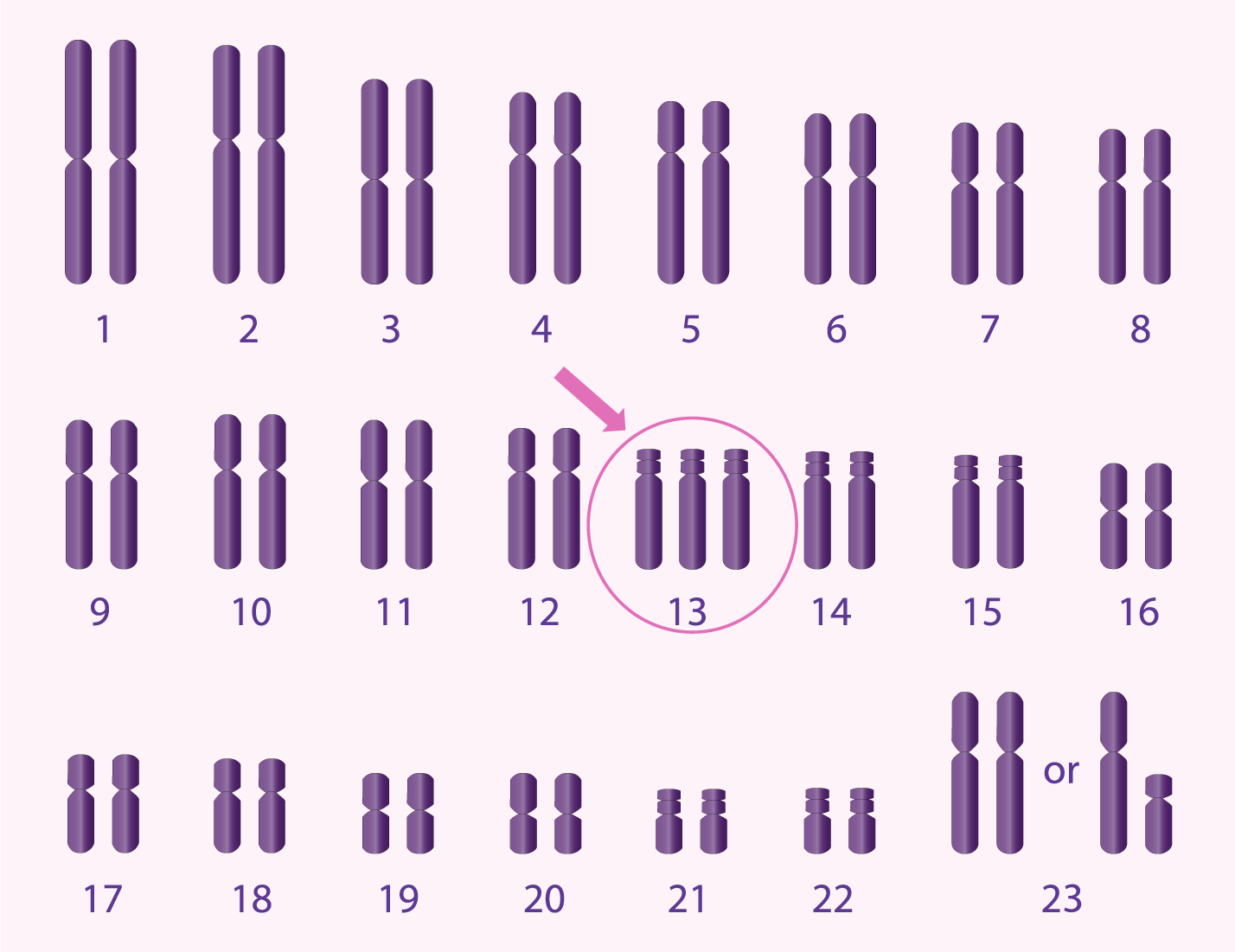
- la trisomie 21 (syndrome de Down)
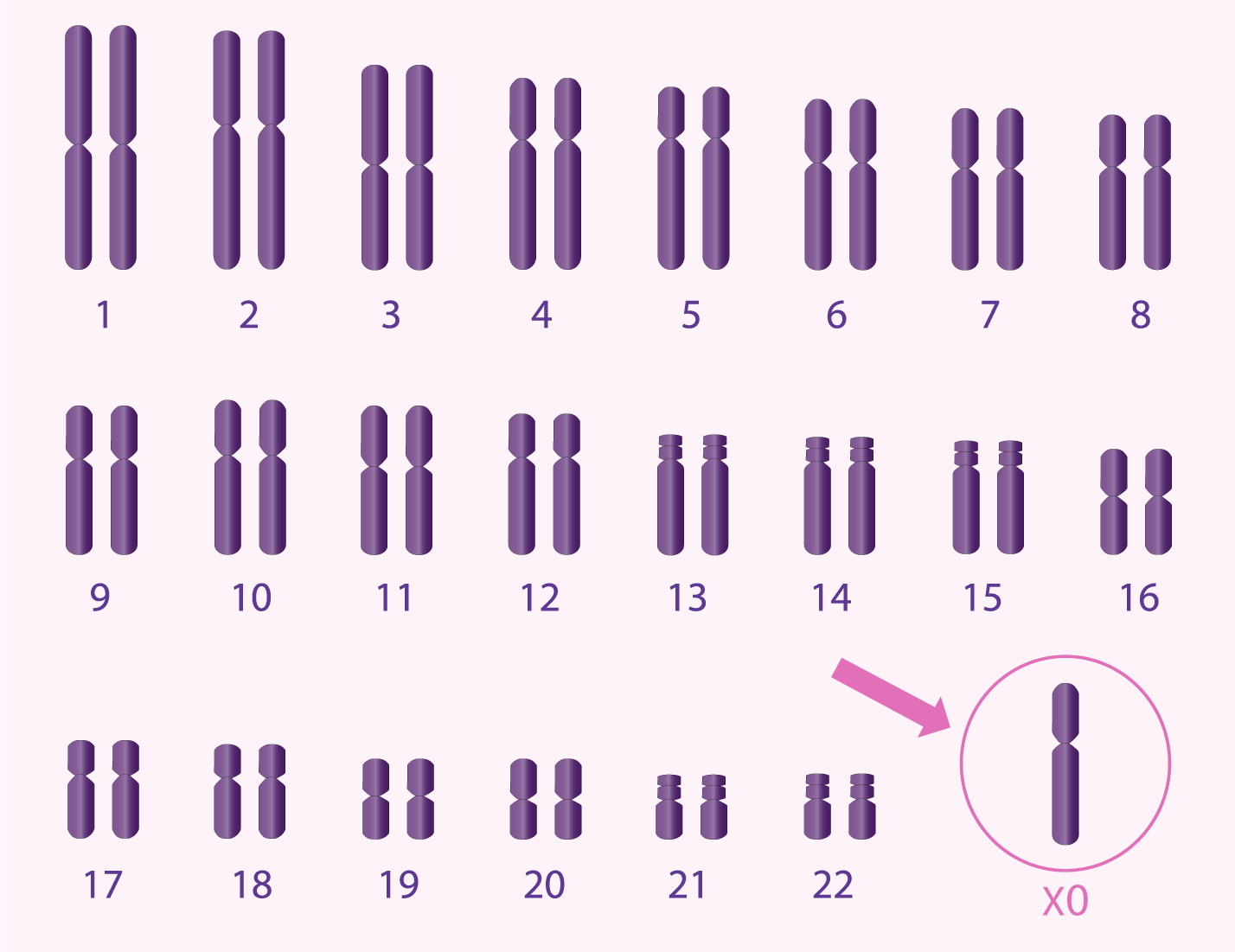
- le syndrome de Turner
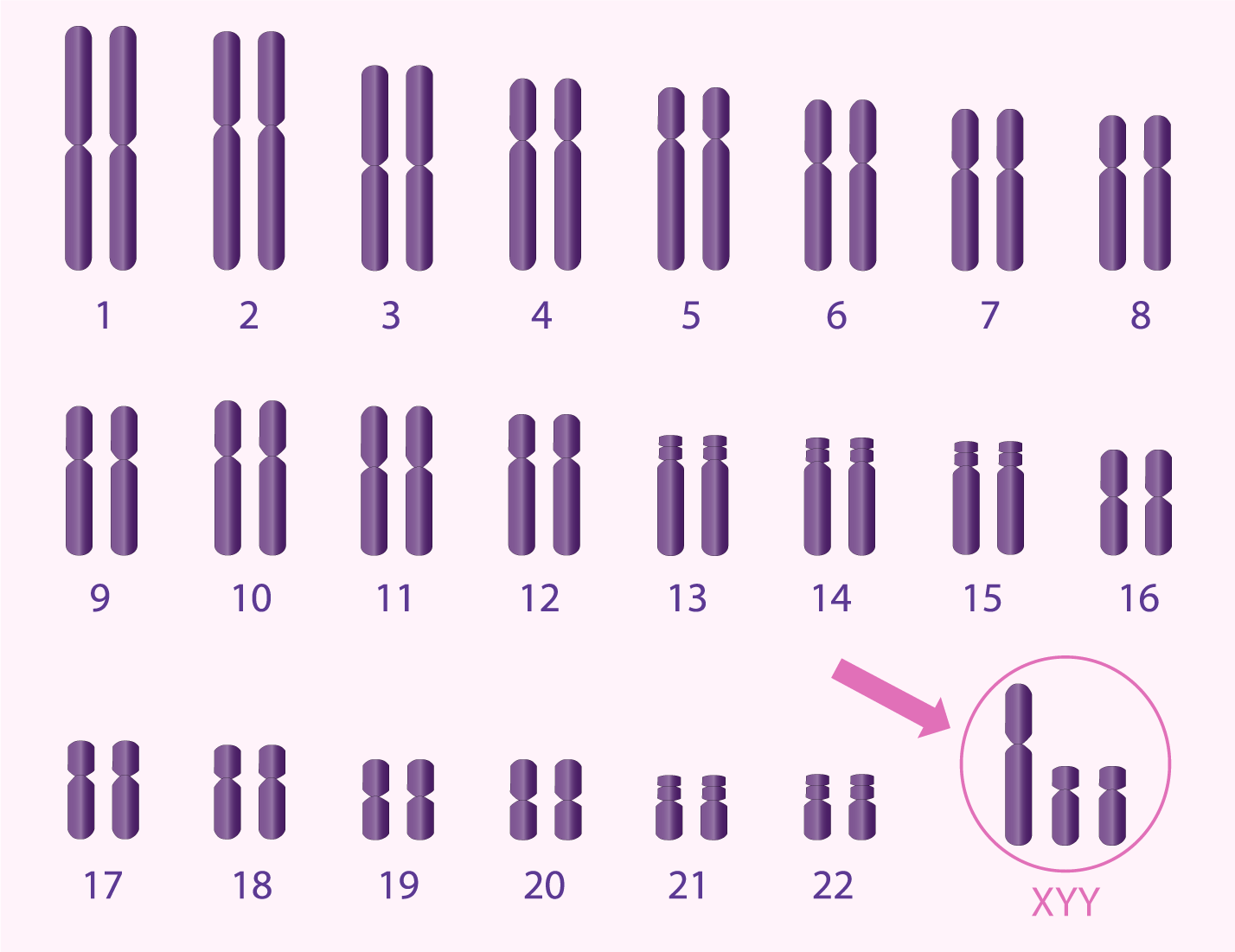
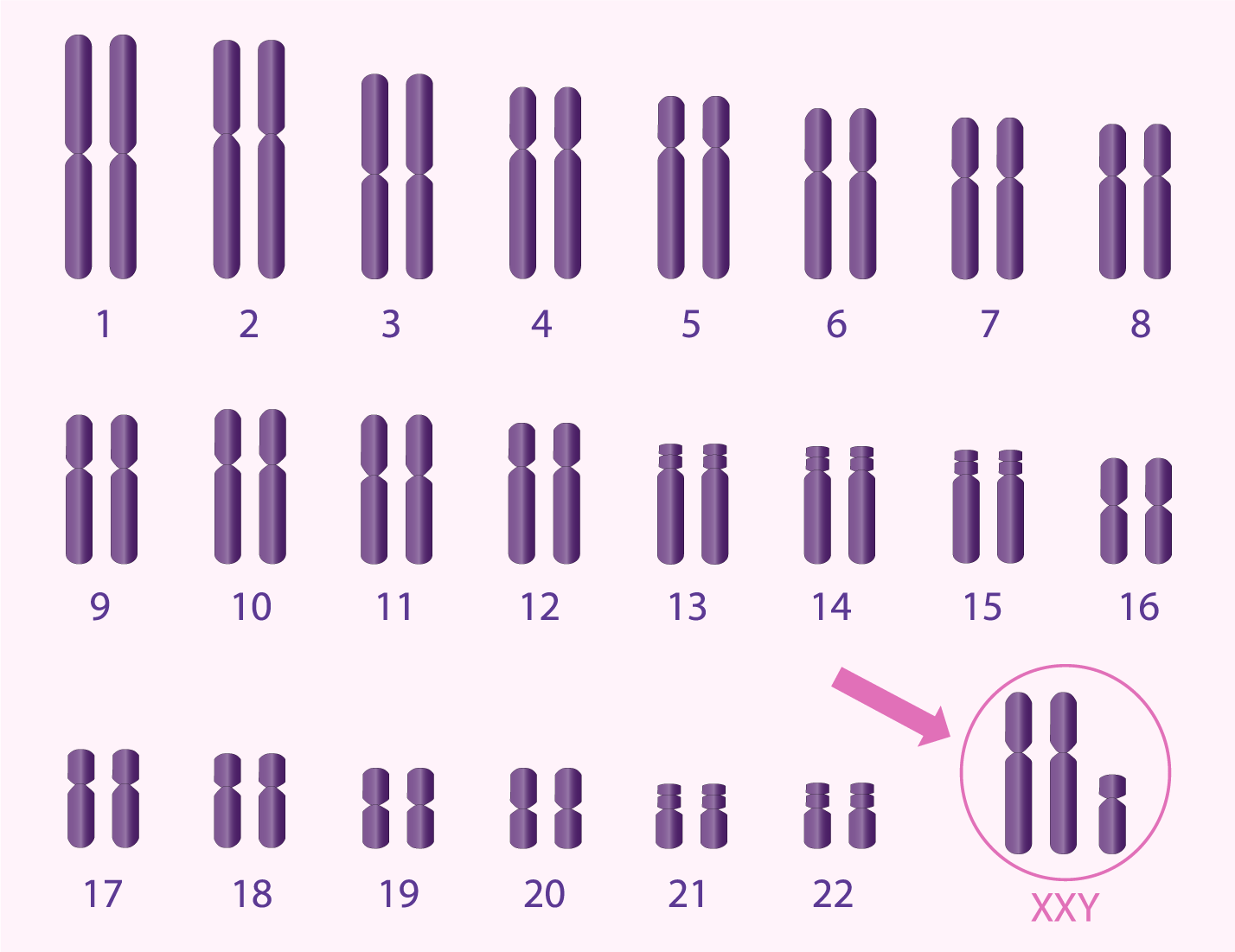
- le syndrome de Klinefelter
Le PGT permet d’identifier ces anomalies avant le transfert embryonnaire.
Le caryotype humain normal
Organisation normale des 23 paires chromosomiques. (Cliquez sur l'image pour agrandir)
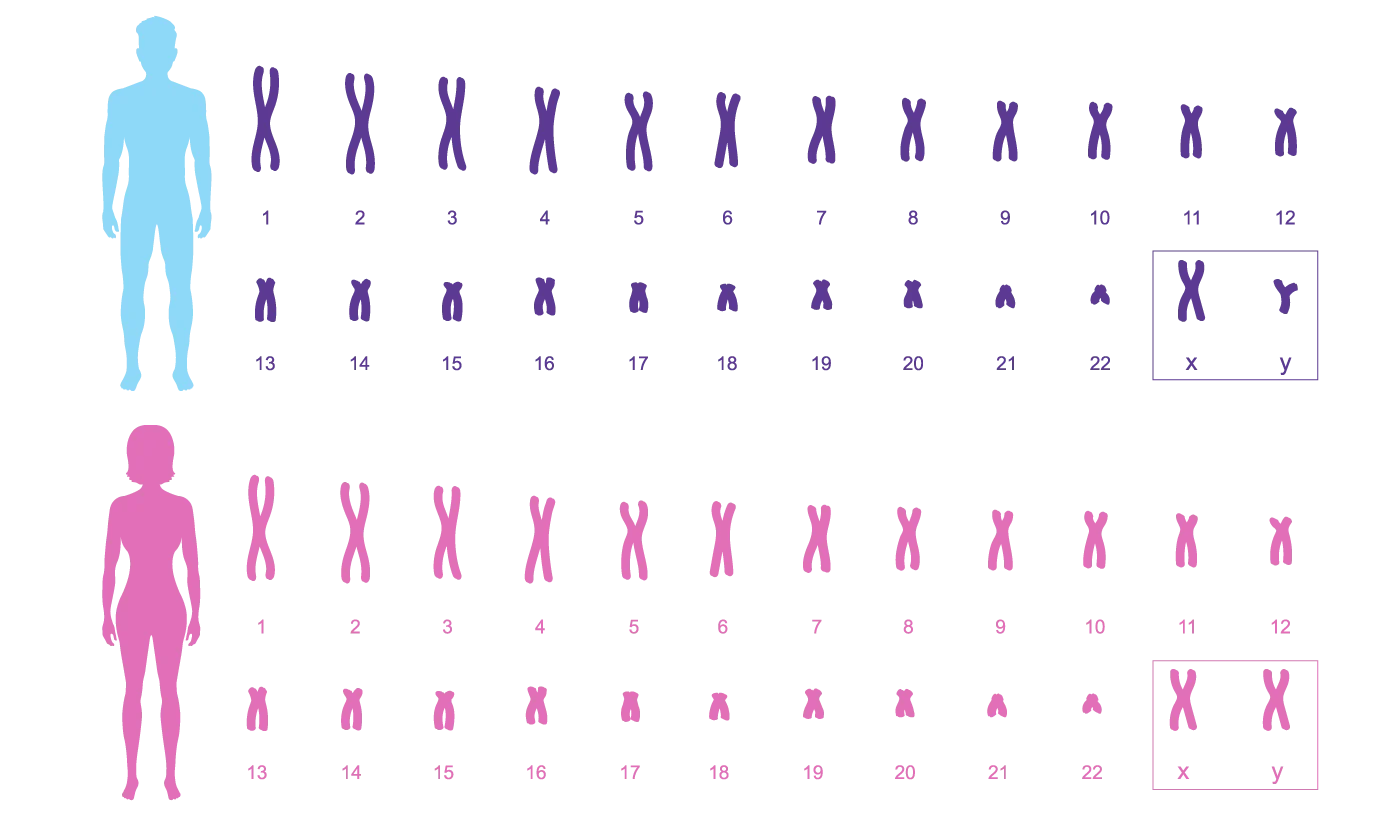
Qui peut bénéficier du diagnostic pré-implantatoire ?
Le diagnostic pré-implantatoire est recommandé dans les situations suivantes :
- Infertilité liée à l’âge maternel (Augmentation du risque d’aneuploïdie après 38 ans).
- Fausses couches répétées (Recherche d’une cause chromosomique embryonnaire).
- Échecs répétés d’implantation en FIV
- Stérilité masculine sévère
- Antécédent d’enfant atteint d’une maladie génétique
- Porteurs connus d’une mutation génétique
- Réarrangements chromosomiques (translocation, inversion)
Le PGT n’est pas systématique. Il répond à une indication clinique précise après évaluation médicale.
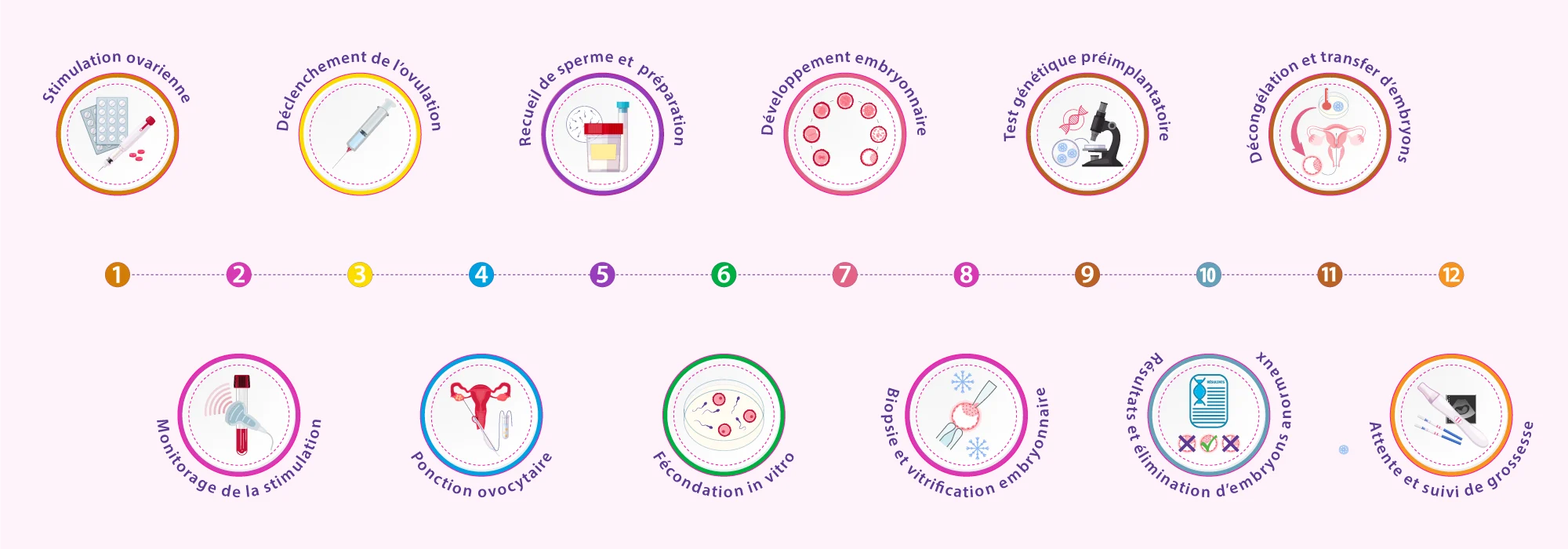
Déroulement d’une FIV avec test génétique préimplantatoire
Le PGT s’intègre dans un cycle classique de FIV, en ajoutant une étape d’analyse génétique des embryons avant leur transfert. Il permet ainsi de sélectionner les embryons chromosomiquement normaux afin d’optimiser les chances d’implantation et de grossesse évolutive.
Schéma détaillé d'une FIV avec biopsie embryonnaire et PGT
Processus complet de FIV incluant l'analyse génétique préimplantatoire. (Cliquez sur l'image pour agrandir)
Les tests génétiques préimplantatoires
Technologies utilisées pour le diagnostic pré-implantatoire
Le PGT repose sur des technologies de génétique moléculaire de haute précision permettant d’analyser les embryons avant leur transfert.
Séquençage de nouvelle génération (NGS) , PGT-A / PGT-SR
Après la fécondation in vitro, les embryons sont cultivés jusqu’au stade blastocyste, une biopsie de quelques cellules est réalisée et les embryons sont cryoconservés afin de permettre l’analyse génétique.
Les cellules prélevées sont ensuite analysées au laboratoire de génétique grâce à la technologie de séquençage de nouvelle génération (Next-Generation Sequencing , NGS), qui permet d’étudier l’ensemble des chromosomes avec une très grande précision.
Cette technologie permet notamment de :
- Amplifier l’ADN à partir de quelques cellules embryonnaires
- Séquencer et analyser des millions de fragments d’ADN
- Comparer les données obtenues au génome humain de référence
- Détecter la présence d’un chromosome supplémentaire, manquant ou toute anomalie chromosomique spécifique
Interprétation des résultats
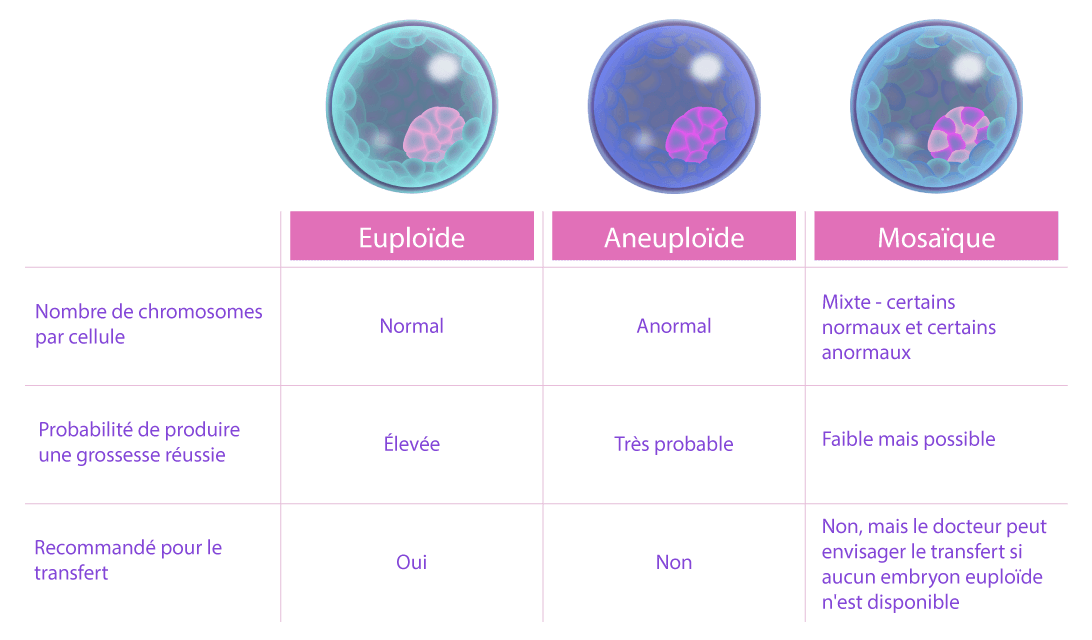
Grâce à des logiciels d’analyse génomique spécialisés, chaque embryon est ensuite classé selon son profil chromosomique :
- Embryons euploïdes : nombre normal de chromosomes, offrant les meilleures chances d’implantation
- Embryons aneuploïdes : anomalie du nombre de chromosomes
- Embryons mosaïques : présence d’un mélange de cellules normales et anormales
Les résultats sont généralement disponibles en 2 à 3 semaines. Votre spécialiste discute ensuite avec vous des embryons présentant le meilleur potentiel d’implantation afin de planifier le transfert embryonnaire dans des conditions optimales.
Karyomapping , PGT-M (maladies monogéniques)
Pour les maladies génétiques spécifiques (comme la thalassémie, l’hémophilie ou certaines dystrophies musculaires), le PGT-M utilise une technique appelée karyomapping :
- Elle identifie quels embryons ont hérité de la mutation génétique familiale.
- Seuls les embryons non affectés sont sélectionnés pour le transfert.
- Le PGT-M peut être réalisé seul ou combiné avec le PGT-A pour optimiser encore les chances de réussite.
Avantages des tests génétiques embryonnaires
- Analyse précise du nombre et de la structure des chromosomes
- Identification des embryons ayant le plus grand potentiel d’implantation
- Réduction du risque de fausses couches
- Transfert d’un seul embryon possible, limitant les grossesses multiples
- Résultats rapides et fiables, disponibles en 2 à 3 semaines
Services
TESTS GÉNÉTIQUES
Diagnostic Pré-Implantatoire (DPI)

Le diagnostic pré-implantatoire (DPI), également appelé PGT (Preimplantation Genetic Testing), est une technologie avancée de génétique reproductive qui permet d'analyser les embryons obtenus par FIV avant leur transfert dans l'utérus.
Objectifs des tests génétiques préimplantatoires
Cette approche permet :
- d'identifier les embryons chromosomiquement normaux
- de prévenir la transmission de maladies génétiques héréditaires
- de réduire le risque de fausses couches
- d'augmenter les taux d'implantation
- d'optimiser les chances de naissance d'un enfant en bonne santé.
Au Centre IRIFIV, le PGT est proposé selon des indications médicales précises et s'intègre dans une stratégie personnalisée et scientifiquement encadrée.
Comprendre les chromosomes et l'aneuploïdie
Chaque embryon humain normal contient 46 chromosomes, organisés en 23 paires : 23 proviennent de l'ovocyte et 23 du spermatozoïde. Une anomalie du nombre de chromosomes est appelée aneuploïdie.
Les embryons aneuploïdes :
- s'implantent difficilement
- sont responsables de nombreuses fausses couches précoces
- peuvent entraîner certaines anomalies congénitales
Le risque d'aneuploïdie augmente avec l'âge maternel. À partir de 38,40 ans, plus de la moitié des embryons peuvent présenter une anomalie chromosomique, expliquant l'augmentation du risque de fausse couche ou de pathologies comme :
- la trisomie 21 (syndrome de Down)
- le syndrome de Turner
- le syndrome de Klinefelter
Le PGT permet d'identifier ces anomalies avant le transfert embryonnaire.
Le caryotype humain normal
Organisation normale des 23 paires chromosomiques. (Cliquez sur l'image pour agrandir)
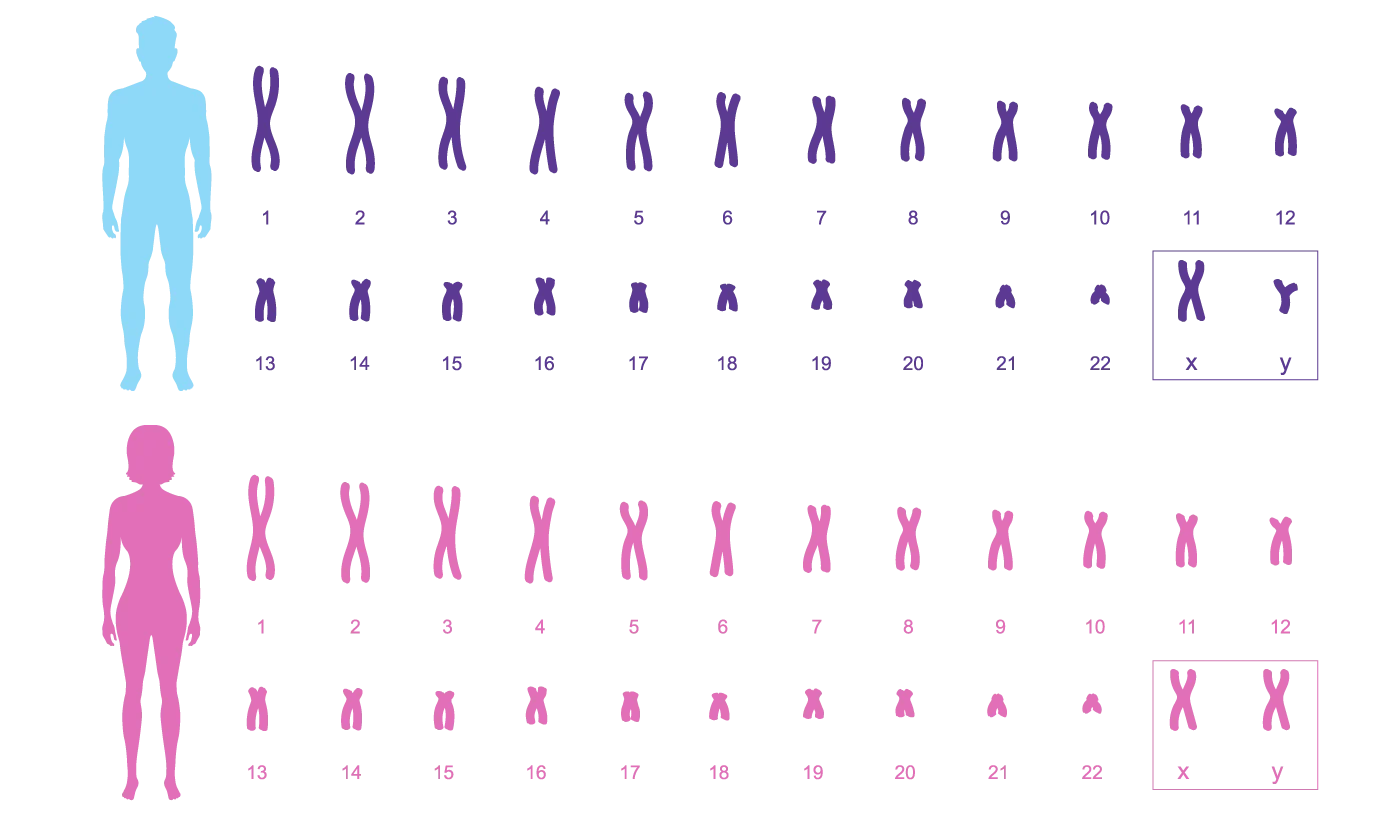
Qui peut bénéficier du diagnostic pré-implantatoire ?
Le diagnostic pré-implantatoire est recommandé dans les situations suivantes :
- Infertilité liée à l'âge maternel (Augmentation du risque d'aneuploïdie après 38 ans).
- Fausses couches répétées (Recherche d'une cause chromosomique embryonnaire).
- Échecs répétés d'implantation en FIV
- Stérilité masculine sévère
- Antécédent d'enfant atteint d'une maladie génétique
- Porteurs connus d'une mutation génétique
- Réarrangements chromosomiques (translocation, inversion)
Le PGT n'est pas systématique. Il répond à une indication clinique précise après évaluation médicale.
Déroulement d'une FIV avec test génétique préimplantatoire
Le PGT s'intègre dans un cycle classique de FIV, en ajoutant une étape d'analyse génétique des embryons avant leur transfert. Il permet ainsi de sélectionner les embryons chromosomiquement normaux afin d'optimiser les chances d'implantation et de grossesse évolutive.
Schéma détaillé d'une FIV avec biopsie embryonnaire et PGT
Processus complet de FIV incluant l'analyse génétique préimplantatoire. (Cliquez sur l'image pour agrandir)
Les tests génétiques préimplantatoires
Technologies utilisées pour le diagnostic pré-implantatoire
Le PGT repose sur des technologies de génétique moléculaire de haute précision permettant d'analyser les embryons avant leur transfert.
Séquençage de nouvelle génération (NGS) , PGT-A / PGT-SR
Après la fécondation in vitro, les embryons sont cultivés jusqu'au stade blastocyste, une biopsie de quelques cellules est réalisée et les embryons sont cryoconservés afin de permettre l'analyse génétique.
Les cellules prélevées sont ensuite analysées au laboratoire de génétique grâce à la technologie de séquençage de nouvelle génération (Next-Generation Sequencing , NGS), qui permet d'étudier l'ensemble des chromosomes avec une très grande précision.
Cette technologie permet notamment de :
- Amplifier l'ADN à partir de quelques cellules embryonnaires
- Séquencer et analyser des millions de fragments d'ADN
- Comparer les données obtenues au génome humain de référence
- Détecter la présence d'un chromosome supplémentaire, manquant ou toute anomalie chromosomique spécifique
Interprétation des résultats
Grâce à des logiciels d'analyse génomique spécialisés, chaque embryon est ensuite classé selon son profil chromosomique :
- Embryons euploïdes : nombre normal de chromosomes, offrant les meilleures chances d'implantation
- Embryons aneuploïdes : anomalie du nombre de chromosomes
- Embryons mosaïques : présence d'un mélange de cellules normales et anormales
Les résultats sont généralement disponibles en 2 à 3 semaines. Votre spécialiste discute ensuite avec vous des embryons présentant le meilleur potentiel d'implantation afin de planifier le transfert embryonnaire dans des conditions optimales.
Karyomapping , PGT-M (maladies monogéniques)
Pour les maladies génétiques spécifiques (comme la thalassémie, l'hémophilie ou certaines dystrophies musculaires), le PGT-M utilise une technique appelée karyomapping :
- Elle identifie quels embryons ont hérité de la mutation génétique familiale.
- Seuls les embryons non affectés sont sélectionnés pour le transfert.
- Le PGT-M peut être réalisé seul ou combiné avec le PGT-A pour optimiser encore les chances de réussite.
Avantages des tests génétiques embryonnaires
- Analyse précise du nombre et de la structure des chromosomes
- Identification des embryons ayant le plus grand potentiel d'implantation
- Réduction du risque de fausses couches
- Transfert d'un seul embryon possible, limitant les grossesses multiples
- Résultats rapides et fiables, disponibles en 2 à 3 semaines